国际创新药闻中国原创ADC获批第五项适应症 2026 年 4 月 10 日,荣昌生物宣布维迪西妥单抗新适应症获国家药品监督管理局正式批准,用于联合特瑞普利单抗治疗 HER2 表达(IHC 1+、2+、3+)的局部晚期或转移性尿路上皮癌患者。
作为全球首个获批一线治疗晚期尿路上皮癌的 HER2-ADC 药物,本次获批填补了全球该领域的治疗空白,标志着维迪西妥单抗从后线治疗正式迈入一线,也成为其在国内获批的第五项适应症。
[微风]新药简介
维迪西妥单抗是靶向 HER2 抗体偶联药物(ADC),本次获批的一线适应症覆盖全 HER2 表达人群,适用范围不再局限于 HER2 过表达患者,免疫组化 1+、2+、3 + 均可使用,且不受顺铂耐受情况限制,大幅拓宽了受益人群边界。
此前维迪西妥单抗已获批胃癌、尿路上皮癌二线、HER2 阳性晚期乳腺伴肝转移、HER2 低表达乳腺癌伴肝转移四项适应症。
[微风]新药有效性
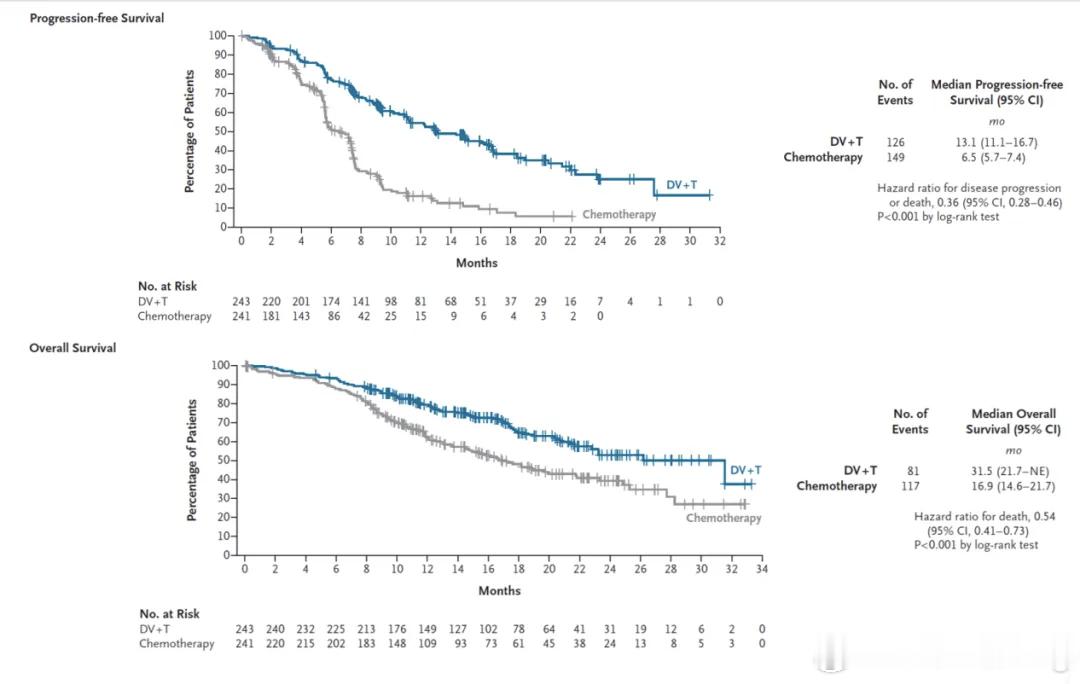
本次获批依据全球首个 HER2 表达晚期尿路上皮癌一线治疗 Ⅲ 期试验 RC48-C016,由北京大学肿瘤医院郭军教授牵头、全国 74 家临床中心参与,共入组 484 例患者,研究成果发表于《新英格兰医学杂志》并亮相 2025 年 ESMO 主席论坛。
截至 2025 年 3 月 31 日,研究达到主要终点:中位无进展生存期 13.1 个月,较含铂化疗组延长一倍,疾病进展或死亡风险降低 64%;
中位总生存期 31.5 个月,较化疗组提升近一倍,死亡风险降低 46%;客观缓解率 76.1%,其中 IHC 1 + 人群缓解率达 65.5%,疾病控制率 91.4%。
中位缓解持续时间 14.6 个月,中位治疗周期 14 个周期,疗效持久且稳定。
安全性方面,联合治疗组与对照组所有不良反应发生率相当,但治疗相关的3级及以上不良反应发生率两组分别为55.1%与86.9%,治疗相关的严重不良反应两组发生率分别为28.4%与40.5%。